|
|
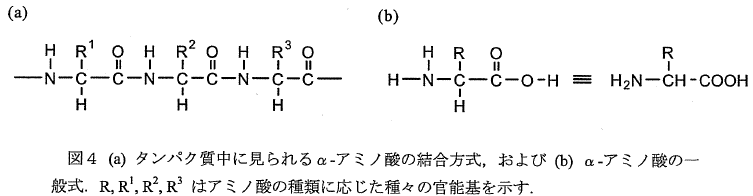
| 問4 Cの図5に示したGFPの蛍光発生部分の構造は、どのようなアミノ酸単位から生じたものかを 推定して答えなさい。図5および解答欄に示した例にならい、残りの部分について、アミノ酸単位 ごとに枠線で囲み、そのアミノ酸の名称を囲んだ枠線の付近に分かりやすく示しなさい。 |
| Location: Home > 挑戦!化学グランプリ! > 1次(筆記) > 緑色蛍光タンパク質GFP ['00-1-5c] |
|
|
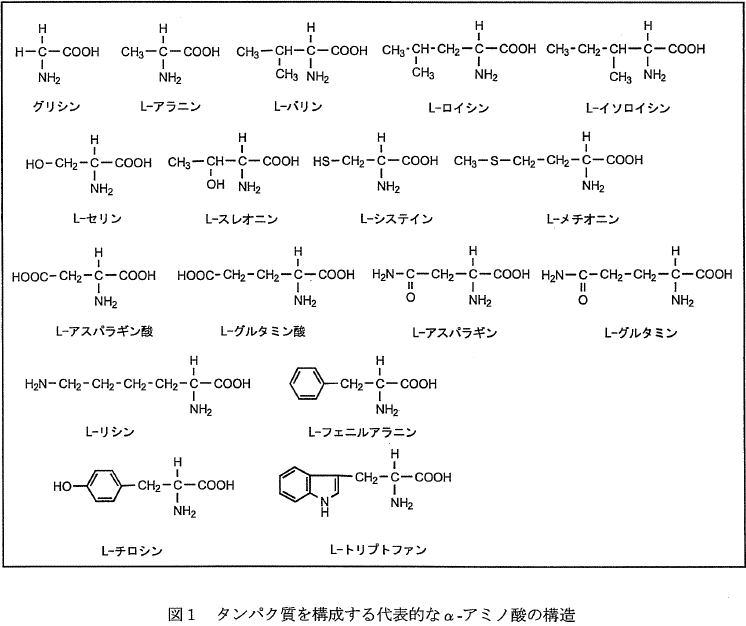
解答欄の図は、おそらく図5と同じ、↑のような図であったと思われます。
問4 問題文中の「ある海生生物」とは、オワンクラゲ
のことですね。
さて、問題の方ですが、解答欄の図と図1と見比べながら、元となるアミノ酸単位を探す問題です。
しかし、いくつかの化学反応が起こっているようです。
問題文より、それらは、
元になるアミノ酸単位中の炭素-炭素結合および窒素-窒素結合はすべて保たれており、切断されるものはない。
ただし、単結合が二重結合に変化しているものがある。また、新たに生成している炭素-窒素結合が1個ある。
であり、それほど大きな変化も起きていないので、
「もととなるアミノ酸はすべて図1に描かれている」のだがら、
図1のアミノ酸一覧表と見比べれば、
だいたい分かりそうですね。
では、見比べてみましょう。
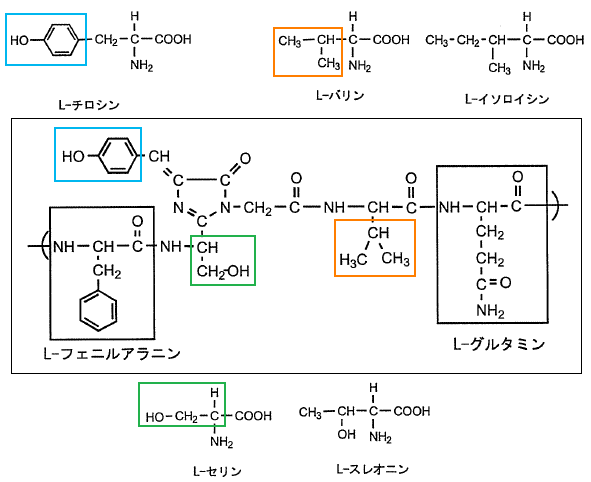
まず、一番最初に目につくのが、水色で囲った部分だ!
ベンゼン環にヒドロキシ基がついたものは、図1より、L-チロシンしかない!
次に、オレンジ色で囲った部分。
炭素の鎖が枝分かれしているぞ!(イソプロピル基)
図1を見てみると、L-バリンかL-ロイシンだろう。
でも、図5とよく見比べてみると、L-ロイシンじゃ、
問題文より、「元になるアミノ酸単位中の炭素-炭素結合は切断されない」んだから、
炭素が1つ多くなっちゃうよね。
じゃあ、L-バリンだ!
次に特徴的な部分は、えーと、5員環部分が、一瞬、L-トリプトファンに見えたが、
よく見ると、ちょっと違った。別のところを探そう。
緑色で囲った部分に着目。
ヒドロキシ基を発見!
図2を見てみると、ヒドロキシ基をもったアミノ酸は、
L-セリン、L-スレオニン、L-チロシンしかないじゃないか!
形をよくよく見ると、元となったのは、L-セリンだと分かった。
そこで、分かったところまでのアミノ酸単位を囲んでみた。
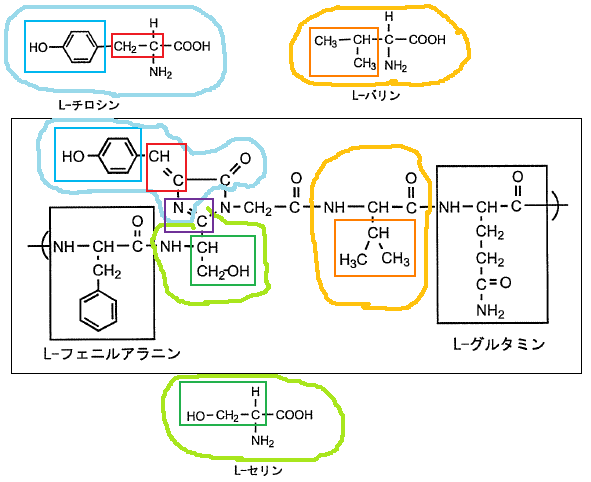
赤四角で囲った部分は、「単結合が二重結合に変化し」た部分だろうけど、
L-セリンが完全に囲むことができない!
カルボキシル基部分の酸素原子が消失してるじゃないか!
やべぇ、間違えたかな、と思い、図1をもう一度見てみるが、やはり、L-セリンで間違いないようだ。
よくよく問題文を見直すと、
「新たに生成している炭素-窒素結合が1個ある」という記述を発見した。
これが紫色で囲んだ部分なのだろう。
ここで、はたと気づいた!
そうだ。これは、「ケトンとアミンの反応による、イミンの生成」である、と。
まあ、答えを確定したいから、これに関しては後で考えることにしよう。
さあ、3つのアミノ酸単位を確定したら、なんか真ん中が余ってしまった。
図1を見ると、これは、グリシンだと分かった。
つまり、この問題の答えは…
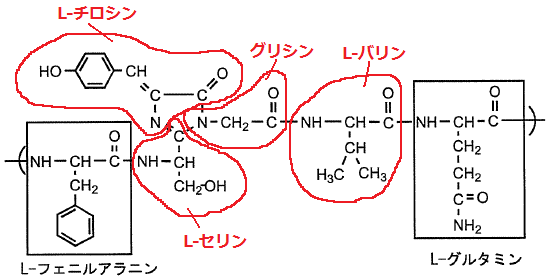
L-セリンをどこまで囲んでいいのかが難しいけど、こんなところで減点はないだろうから、
微妙にC=N結合に食い込ませておけばいいだろう。
……という風に、実況中継風に解説してみました。
<補足:イミンの合成法>
イミンとは、C=N結合をもつ、R1-C(=NR3)-R2
の一般式で与えられる化合物の総称です。
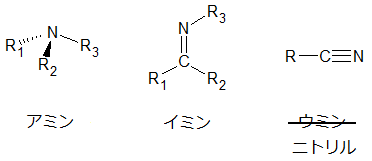
一番左の「アミン」は、高校化学でもおなじみの有機化合物ですが、
C=N結合が出現すると、「イミン」と呼ばれるようになります。
では、アミン、イミンときたから、C≡N結合をもてば、「ウミン」か? と思うところなのですが、
残念。-C≡Nはシアノ基(ニトリル基)です。シアノ基(ニトリル基)を持つ一般に「ニトリル」と呼ばれますね。
さて、そんなイミンですが、どうやって合成するのか、と言うと、
一般に、アルデヒドやケトンに、アンモニアや第一級アミンを、酸触媒の存在下で付加させ、
中間生成物のアミノアルコールから水が脱離することにより生成します。
まとめると、カルボニル化合物とアミンが脱水縮合して得られるということです。
図で説明しますと、
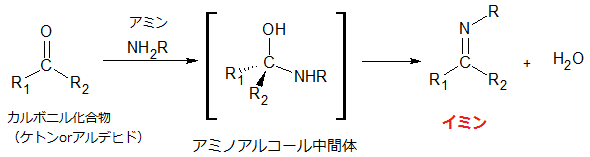
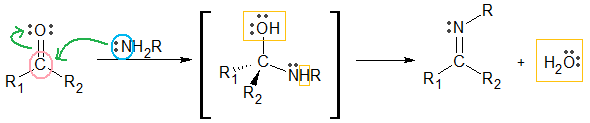
求核性のアミンが求電子性をもったカルボニル基(の炭素原子)に求核付加
し、
付加体のアミノアルコールから、水(オレンジ色で囲んだ部分)が脱離して、
イミンが生成するというわけです。
有機化学にたしなみのある人なら納得できるでしょうが、
そうでない人には、サッパリでしょうね、わかります。
まず、求核性、求電子性って何よ? っていう方へ。
幸いなことに、この辺を扱った問題が、化学グランプリの過去問にあります。
実際に問題を解きながら理解するといいでしょう。
→化学グランプリ
'07 2-a ラジカル反応とイオン反応
とにかく、今スグに「求核性」「求電子性」の意味を知りたい方へ。
平たく言えば、
「求核性」=「マイナスの極性をもつ」
「求電子性」=「プラスの極性をもつ」
ということです。
「求核付加」とは、「求核的な付加反応」のことです。(そのまんま)
しかし、上の図の反応機構は、途中の細々とした反応をひたすら省略してあるので、
これで十分ではありません。
この辺の詳しい機構は、「有機化学の部屋」の方でやってくれると思います。
私の管轄外なので、今はなんとも言えませんが。
一つ一つの反応を突き詰めていくことは有機化学の醍醐味です。
ちょっとでも有機化学に興味を持った方は、
「化学グランプリに役立つ参考書群(仮題)」(準備中…)
で紹介する有機化学関連の本を読んでみることをオススメします。
以上が、2000年度の「GFP」に関する問題でした。
GFPに関する問題というよりは、構成アミノ酸をただ探すだけの問題で、
深いところまで踏み込んでいない問題でした。
ただし、これはノーベル賞受賞前の話です。
さて、ということは、2009年度以降の化学グランプリの問題に、「GFP」が取り上げられる可能性は高い?
GFPの詳細については、近々「ノーベル賞でつづる化学史」の方で。
お楽しみに!
|
|
||